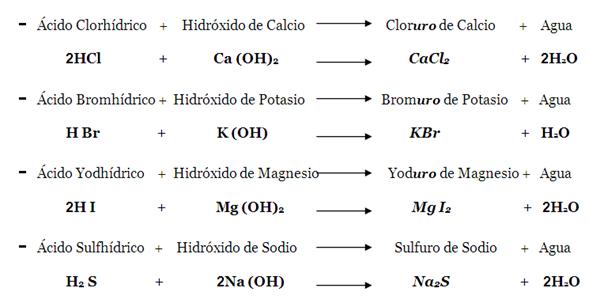
Estequiometria
Es el conjunto de cálculos cuantitativos que se pueden ver expresados en una reacción química, los miembros de este conjunto son:
- masa
- moléculas
- mol
- átomo
- peso molecular
- átomo gramo
- densidad
- pureza
- eficiencia
- volumen
estos miembros del conjunto de la estequimetria son nombrados factores estequiometricos.
- pagina tutora sobre estequiometria: http://www.eis.uva.es/~qgintro/esteq/tutorial-02.html
- video con apoyo conceptual basico sobre el tema: https://www.youtube.com/watch?v=QDTn__99GpI